Cristalización de CuSO4
Es un trabajo orientado al alumnado de los niveles más bajos como introducción a la separación y purificación de sustancias.
En el mismo, se aprovecha la preparación de una cristalización de CuSO4 para hacer una
disolución de concentración conocida en g/l y una filtración.
Enlace al guión de laboratorio.




Material- Tetraoxosulfato (VI) de cobre- Vaso de precipitado - Matraz aforado de 100 ml - Embudo y papel de filtro - Balanza - Cristalizador o plato de plástico - Agua destilada - Mechero Bunsen |
.
- Dada la naturaleza del experimento es razonable utilizar sulfato de cobre de baja calidad. El utilizado en agricultura para el tratamiento
de los hongos de la vid funciona perfectamente. |
Comentarios a la preparación del montaje
El sulfato de cobre no se disuelve con facilidad. Si los cristales son gruesos, conviene triturarlos previamente en un mortero y calentar el agua para disolverlos.
Aunque interesa hacer una disolución muy concentrada, la solubilidad del sulfato de cobre es de 20,7 g/100 ml a 20ºC, de ahí que se proponga una disolución de 100g/litro.
Aumentar la concentración dificulta la disolución.
Normalmente la disolución de sulfato de cobre elaborada no tiene impurezas filtrables, la filtración inicial se hace como procedimiento normalizado de preparar una
cristalización y es, evidentemente, un paso que se puede omitir.
Es importante utilizar agua destilada, el agua del grifo produce cristales blancos en los bordes de los azules.
Como el proceso de cristalización debe ser lento y dura varios días, es conveniente dejar los platos en un lugar fuera de la zona habitual de trabajo,
como lo alto de un armario aunque, en este caso, no es raro que la disolución se derrame al subir o al bajar.
Como el plato estará varios días evaporando, es conveniente cubrirlo con un papel que impida la caída de polvo pero permita la evaporación.
La evaporación debe ser lenta para obtener buenos cristales, no conviene un sitio muy ventilado.
Aspectos didácticos
Este trabajo pretende:
- Preparar disoluciones de concentración conocida en g/litro.
- Utilizar la cristalización como método de separación y purificación de sustancias.
- Relacionar la forma de los cristales con la estructura interna de la materia que los componen.
A los alumnos de menor edad les suele paracer muy sorprendente que los cristales se formen con formas regulares sin intervención humana.
Para muchos de ellos, las formas regulares son artificiales. Es buen momento para recordar los conceptos de los sólidos cristalinos,
que suelen conocer pero no aplican.
Es importante asociar la lentitud de la cristalización con la obtención de mejores cristales relacionándolo con la entrada ordenada de partículas
en la estructura cristalina. Es interesante poner una parte de la disolución sobrante y evaporarla hasta sequedad en un vaso, para poder comparar
el residuo seco obtenido rápidamente con los cristales obtenidos lentamente.
Si se dipone de cristales pequeños de un experimento anterior, es muy didáctico sembrar alguno en un lateral del plato para ver su evolución
y diferenciarlo de los que se forman sin sembrado.
El calentamiento de un cristal para eliminar el agua de cristaliación sirve para hacer ver que el agua se puede quedar en la estructura cristalina
y que un cristal aparentemente seco contiene agua. Al hacer el experimento en un tubo de ensayo, el agua es fácilmente visible al condensar
en las paredes del tubo.
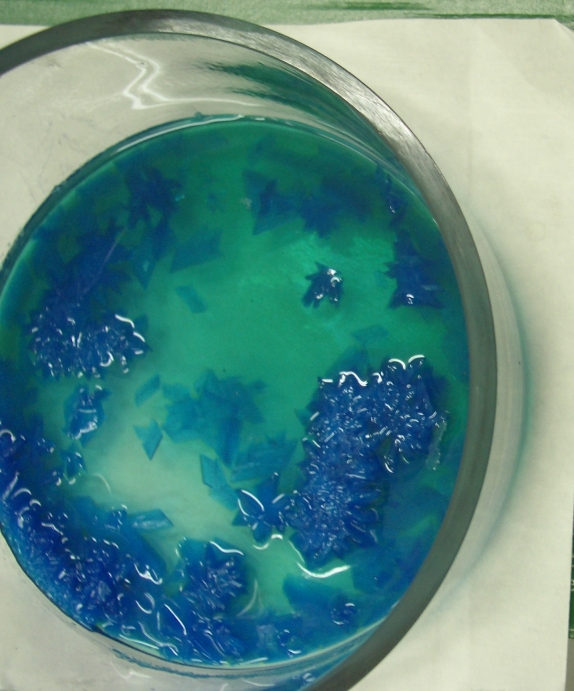 Cristalización avanzada |
 Cristal de gran tamaño obtenido con siembra |

